Что такое серная кислота в химии. Сернистая кислота это
H2SO3, слабая двухосновная кислота. В свободном виде не выделена, существует в водных растворах. Соли сернистой кислоты сульфиты … Большой Энциклопедический словарь
СЕРНИСТАЯ КИСЛОТА - (H2SO3) слабая двухосновная кислота. Существует лишь в водных растворах. Соли С. к. сульфиты. Применяют в целлюлозно бумажной и пищевой промышленности. См. также Кислоты и ангидриды … Российская энциклопедия по охране труда
сернистая кислота - — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN sulfurous acid … Справочник технического переводчика
Н2SO3, слабая двухосновная кислота. В свободном виде не выделена, существует в водных растворах. Соли серной кислоты сульфиты. * * * СЕРНИСТАЯ КИСЛОТА СЕРНИСТАЯ КИСЛОТА, H2SO3, слабая двухосновная кислота. В свободном виде не выделена,… … Энциклопедический словарь
сернистая кислота - sulfito rūgštis statusas T sritis chemija formulė H₂SO₃ atitikmenys: angl. sulfurous acid rus. сернистая кислота ryšiai: sinonimas – vandenilio trioksosulfatas (2–) … Chemijos terminų aiškinamasis žodynas
H2SO3, слабая двухосновная кислота, отвечающая степени окисления серы +4. Известна только в разбавленных водных растворах. Константы диссоциации: K1 = 1,6 · 10 2, K2 = 1,0 · 10 7 (18°C). Даёт два ряда солей: нормальные Сульфиты и кислые… … Большая советская энциклопедия
H2SO3, слабая двухосновная кислота. В свободном виде не выделена, существует в вод. р рах. Соли С. к. сульфиты … Естествознание. Энциклопедический словарь
См. Сера … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Диоксид (двуокись) серы образуется при сжигании серы в воздухе или кислороде. Он получается также при прокаливании на воздухе («обжигании») сульфидов металлов, например железного колчедана:
По этой реакции диоксид серы получают обычно в промышленности (о других промышленных способах получения см, 9 § 131).
Диоксид серы - бесцветный газ («сернистый газ») с резким эапахом горячей серы. Он довольно легко конденсируется в бесцветную жидкость, кипящую при . При испарении жидкого происходит сильное понижение температуры (до ).
Диоксид серы хорошо растворяется в воде (около 40 объемов в 1 объеме воды при ); при этом частично происходит реакция с водой и образуется сернистая кислота:
Таким образом, диоксид серы является ангидридом сернистой кислоты. При нагревании растворимость уменьшается и равновесие смещается влево; постепенно весь диоксид серы снова выделяется из раствора.
Молекула построена аналогично молекуле озона. Ядра составляющих ее атомов образуют равнобедренный треугольник:
Здесь атом серы, как и центральный атом кислорода в молекуле озона, находится в состоянии -гибридизации и угол близок к . Ориентированная перпендикулярно к плоскости молекулы -орбиталь атома серы не участвует в гибридизации. За счет этой орбитали и аналогично ориентированных -орбиталей атомов кислорода образуется трехцентровая -связь; осуществляющая ее пара электронов принадлежит всем трем атомам молекулы.
Диоксид серы применяют для получения серной кислоты, а также (в значительно меньших количествах) для беления соломы, шерсти, шелка и как дезинфицирующее средство (для уничтожения плесневых грибков в подвалах, погребах, винных бочках, бродильных чанах).
Сернистая кислота - очень непрочное соединение. Она известна только в водных растворах. При попытках выделить сернистую кислоту она распадается на и воду. Например, при действии концентрированной серной кислоты на сульфит натрия вместо сернистой кислоты выделяется диоксид серы:
Раствор сернистой кислоты необходимо предохранять от доступа воздуха, иначе она, поглощая из воздуха кислород, медленно окисляется в серную кислоту:
Сернистая кислота - хороший восстановитель. Например, свободные галогены восстанавливаются ею в галогеноводороды:
![]()
Однако при взаимодействии с сильными восстановителями сернистая кислота может играть роль окислителя. Так, реакция ее с сероводородом в основном протекает согласно уравнению:
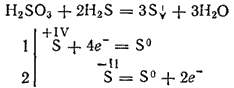
Будучи двухосновной , сернистая кислота образует два ряда солей. Средние ее соли называются сульфитами, кислые - гидросульфитами.
Как и кислота, сульфиты и гидросульфиты являются восстановителями. При их окислении получаются соли серной кислоты.
Сульфиты наиболее активных металлов при прокаливании разлагаются с образованием сульфидов и сульфатов (реакция самоокисления - самовосстановления):
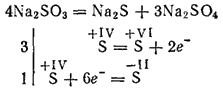
Сульфиты калия и натрия применяются для отбеливания некоторых материалов, в текстильной промышленности при крашении тканей, в фотографии. Раствор (эта соль существует только в растворе) применяется для переработки древесины в так называемую сульфитную целлюлозу, из которой потом получают бумагу.
Сернистая кислота способна реагировать с кислородом. При этом образуется серная кислота. Такая реакция протекает очень долго и возможна только при нарушении правил хранения. Сернистая кислота обладает как окислительными, так и восстановительными свойствами. С ее помощью можно получать галогенные кислоты. Водный раствор при реакции с хлором образует соляную и серную кислоту.
При реакции с сильными восстановителями сернистая кислота играет роль окислителя. Одним из таких веществ является сероводород, газ с очень неприятным запахом. Взаимодействуя с водным раствором серной кислоты, он образует серу и воду. Соли сернистой кислоты также обладают восстановительными свойствами. Они делятся на сульфиты и гидросульфиты. При реакциях окисления этих солей образуется серная кислота.
Получение сернистой кислоты
Сернистая кислота образуется только при взаимодействии сернистого газа и воды. Нужно получить сернистый газ. Это можно сделать при помощи меди и серной кислоты. Осторожно налейте концентрированную серную кислоту в пробирку и бросьте туда кусочек меди. Нагрейте пробирку при помощи спиртовки.
В результате нагревания образуется медный купорос (сульфат меди), вода и сернистый газ, который при помощи специальной трубочки нужно подвести к колбочке с чистой водой. Таким образом можно получить сернистую кислоту.
Помните, что сернистый газ вреден для человека. Он вызывает поражение дыхательных путей, потерю аппетита и головную боль. Длительное вдыхание может вызвать обморочное состояние. При работе с ним нужна осторожность.
Применение сернистой кислоты
Сернистая кислота обладает антисептическими свойствами. Ее применяют при обеззараживании поверхностей, ферментации зерна. С ее помощью можно отбелить некоторые вещества, которые при взаимодействии с сильными окислителями (например, хлором) разлагаются. К таким веществам относится шерсть, шелк, бумага и некоторые другие. Ее антибактериальные свойства используются для предотвращения брожения вина в бочках . Таким образом благородный напиток может храниться очень долго, приобретая благородный вкус и неповторимый аромат.
Сернистую кислоту используют при производстве бумаги. Добавление этой кислоты входит в технологию получения сульфитной целлюлозы. Затем ее обрабатывают раствором гидросульфита кальция, чтобы связать волокна воедино.
Возможно, будет полезно почитать:
- Патриарх кирилл запретил актеру и священнику ивану охлобыстину служить в церкви Охлобыстин церковный сан ;
- Иван охлобыстин - биография, информация, личная жизнь Почему охлобыстин ушел из священников ;
- Ужин для ребенка 4 лет рецепты меню ;
- Принципы функционирования бюджетной системы РФ ;
- Особенности размещения населения на территории земли Население земли размещается равномерно средняя плотность населения ;
- Тонька-пулеметчица — cтрашная судьба страшного человека Фильм палач тонька пулеметчица реальная история ;
- Как поздравить начальницу с юбилеем? ;
- Российские студенты выиграли чемпионат мира по программированию Вот они, герои ;